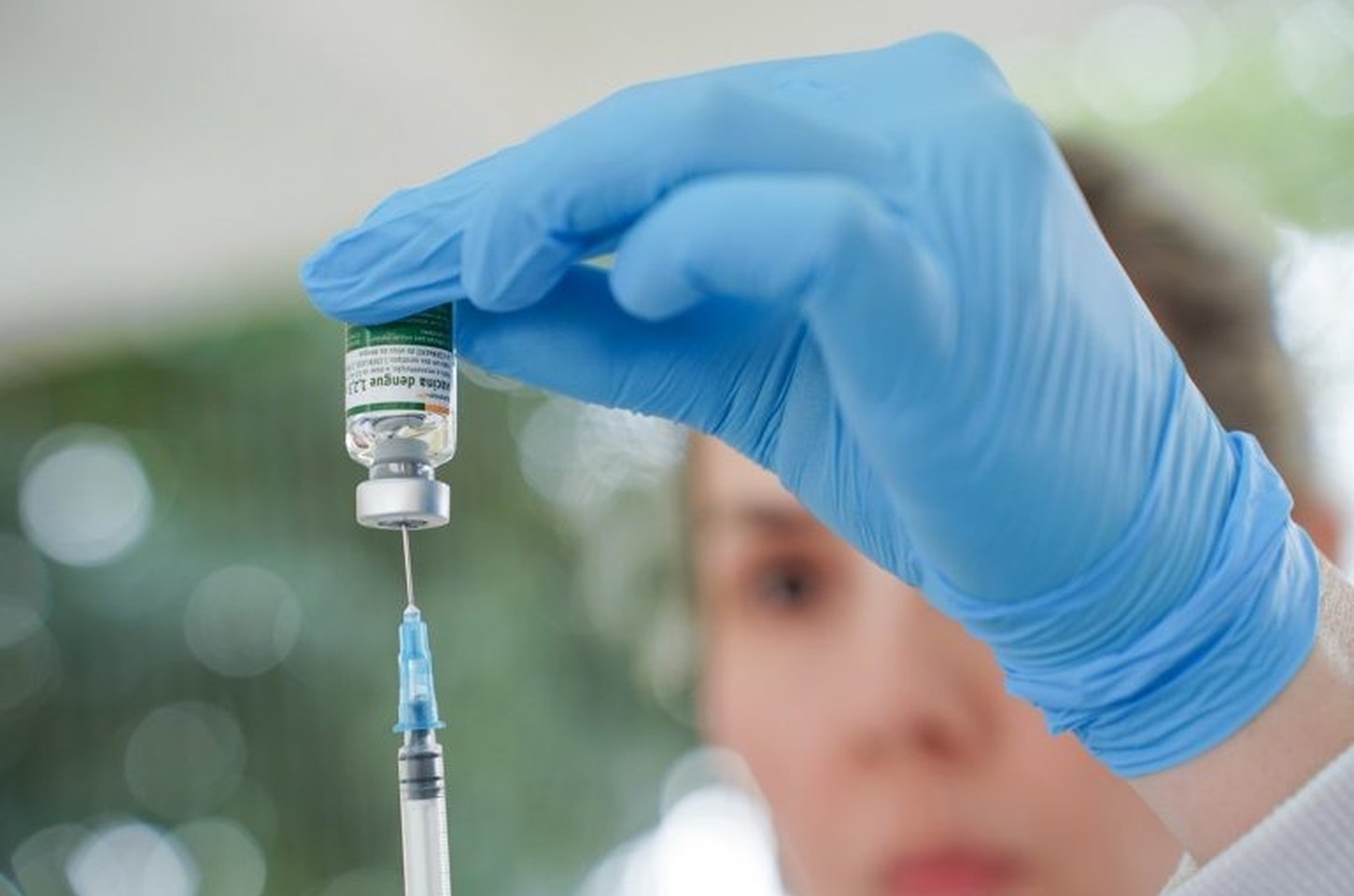
A história da vacina brasileira contra a dengue começou em 2006, quando o cientista Isaías Raw (1927-2022), então ex-diretor do Instituto Butantan e da Fundação Butantan, convocou uma reunião que mudaria o curso da saúde pública no país. Naquele ano, a dengue atingia níveis históricos nas Américas, com 260 mil casos prováveis só no Brasil, e Raw enxergava a necessidade urgente de um imunizante nacional para proteger a população.
O pontapé inicial veio com pesquisadores do Instituto Nacional de Alergia e Doenças Infecciosas (NIAID), parte dos Institutos Nacionais de Saúde (NIH) dos Estados Unidos, que foram convidados para apresentar a tecnologia que vinham desenvolvendo para uma candidata vacinal contra a doença. Essa conversa inicial se transformaria em uma parceria científica que atravessaria duas décadas.
A colaboração foi oficializada em 2009, quando o NIH/NIAID cedeu ao Butantan as cepas atenuadas dos quatro sorotipos do vírus da dengue (DENV-1, DENV-2, DENV-3 e DENV-4). A tecnologia licenciada era fruto de uma década de pesquisa nos EUA e mais de 30 ensaios clínicos de fase 1, necessários para identificar a melhor forma de atenuar cada um dos quatro vírus.
"Se a vacina não induz imunidade contra os quatro vírus, nós podemos acabar predispondo a pessoa a ter uma dengue mais grave no futuro, caso ela seja infectada", explica Anna Durbin, cientista e diretora do Centro de Pesquisa em Imunizações da Universidade Johns Hopkins, que conduziu os ensaios clínicos em parceria com o NIH/NIAID. Essa preocupação com a segurança, especialmente em pessoas que nunca tiveram dengue, norteou os pesquisadores do início ao fim do projeto.
O desenvolvimento da vacina apresentou desafios únicos. Diferentemente de outras vacinas virais, era necessário criar um imunizante que protegesse simultaneamente contra os quatro tipos do vírus da dengue. Stephen Whitehead, cientista sênior do Laboratório de Doenças Virais do NIH/NIAID que liderou o desenvolvimento das cepas atenuadas, explica que "nós customizamos as mutações genéticas para cada vírus, a fim de obter os candidatos monovalentes mais satisfatórios".
Cada cepa foi testada separadamente em modelos animais e, depois, em seres humanos. Foram necessários quatro testes clínicos só com o componente DENV-4, por exemplo, para descobrir a dosagem ideal. "No caso do sorotipo 4, começamos com uma quantidade de 100.000 partículas de vírus, e acabamos descobrindo que apenas 1.000 partículas eram suficientes para induzir resposta", detalha Anna Durbin.
Na etapa final, os cientistas norte-americanos chegaram a duas formulações tetravalentes (TV003 e TV005). Um novo ensaio clínico determinou que a TV003, com uma única dose, gerou anticorpos contra os quatro tipos da dengue em 90% dos voluntários e apresentou melhor perfil de segurança. Foi com base nessa formulação que o Instituto Butantan desenvolveu sua própria versão da vacina entre 2009 e 2012.
"O Butantan teve confiança no produto antes mesmo de termos uma formulação final", afirma Stephen Whitehead. "É uma instituição que tem um histórico muito consolidado em desenvolvimento de vacinas, e sempre soubemos que seria uma parceria que daria certo".
Os ensaios clínicos de fase 3 no Brasil contaram com 16 mil voluntários de diferentes regiões do país. Metade dos participantes tinha histórico de dengue, e a outra metade nunca havia tido contato com o vírus. Em cinco anos de acompanhamento, não foram observados sinais de preocupação em nenhum dos grupos, e a vacina demonstrou alta proteção contra dengue grave e com sinais de alarme, na faixa de 90%.
Uma das grandes vantagens da Butantan-DV é ser aplicada em dose única. "As vacinas não protegem as pessoas; o que protege é a vacinação", ressalta Anna Durbin. "E com dose única, a vacina vai mais longe – você pode imunizar muito mais pessoas e não precisa se preocupar se elas voltam ao posto para receber a segunda dose. Elas já estarão protegidas".
Os cientistas acreditam que o imunizante, combinado a estratégias de controle do mosquito Aedes aegypti, poderá reduzir significativamente o número de casos e hospitalizações por dengue no Brasil nos próximos anos. "Esse trabalho foi da bancada ao produto e agora, com o Instituto Butantan, está indo além", destaca Stephen Whitehead. "Nos últimos 20 anos, diretoria após diretoria, nós estivemos aqui anualmente e o Butantan continuou levando esse projeto para frente e entendendo sua importância, porque é uma instituição comprometida com a saúde dos brasileiros".
Anna Durbin reforça o impacto global que a vacina pode ter: "Metade da população mundial vive em áreas de risco para dengue, e quando conseguirmos imunizar todo o público de risco, acredito que teremos um dos maiores impactos já vistos contra uma doença viral".
A Butantan-DV foi aprovada pela Agência Nacional de Vigilância Sanitária (Anvisa) em novembro de 2025 para o público de 12 a 59 anos, e começou a ser aplicada em janeiro deste ano. A vacinação foi iniciada nos municípios de Nova Lima (MG), Maranguape (CE) e Botucatu (SP), em um projeto piloto, e depois expandida para profissionais de saúde da Atenção Primária.
Durante as celebrações dos 125 anos do Instituto Butantan, Stephen Whitehead e Anna Durbin foram homenageados por suas contribuições no desenvolvimento da Butantan-DV. "A Butantan-DV é resultado do esforço não de uma só pessoa, de um só grupo, mas de um universo de pessoas que trabalharam diariamente por duas décadas para fazê-la acontecer", resumiu Esper Kallás, diretor do Instituto Butantan.
Os pesquisadores também destacam a importância fundamental dos voluntários dos ensaios clínicos. "São pessoas que doaram seu tempo, confiaram nos investigadores e acreditaram na ciência", diz Anna Durbin. "Eles fizeram isso pelo bem da saúde pública e devemos nossos agradecimentos a eles".
Atualmente, o Instituto Butantan conduz um ensaio clínico para avaliar a vacina na população de 60 a 79 anos, enquanto a expectativa é que, futuramente, o imunizante também possa ser disponibilizado para crianças de 2 a 6 anos – faixa etária que demonstrou resultados promissores de segurança e eficácia durante a fase 3 dos testes.